Transplantation hépatique pédiatrique
Pour en savoir plus sur la transplantation hépatique aux HUG, vous pouvez consulter :
Rue Gabrielle-Perret-Gentil 4
1205 Genève
Suisse

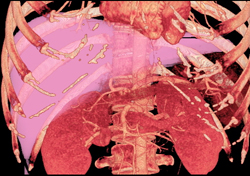 La transplantation hépatique est le remplacement du foie malade par un foie sain provenant d'un donneur humain (allogreffe) vivant ou décédé. La technique la plus couramment utilisée est la transplantation orthotopique, dans laquelle le foie natif est enlevé et l'organe du donneur transplanté dans le même emplacement anatomique. La transplantation hépatique est aujourd'hui une option thérapeutique unanimement acceptée pour pallier tant aux hépatopathies en phase terminale qu'aux insuffisances hépatiques aiguës. Elle est également l'un des traitements les plus coûteux de la médecine moderne.
La transplantation hépatique est le remplacement du foie malade par un foie sain provenant d'un donneur humain (allogreffe) vivant ou décédé. La technique la plus couramment utilisée est la transplantation orthotopique, dans laquelle le foie natif est enlevé et l'organe du donneur transplanté dans le même emplacement anatomique. La transplantation hépatique est aujourd'hui une option thérapeutique unanimement acceptée pour pallier tant aux hépatopathies en phase terminale qu'aux insuffisances hépatiques aiguës. Elle est également l'un des traitements les plus coûteux de la médecine moderne.
La première greffe de foie humain a été réalisée en 1963 à Denver aux États-Unis par une équipe chirurgicale dirigée par le Dr Thomas Starzl. Celui-ci a réalisé plusieurs transplantations successives au cours des années suivantes avant qu'un premier succès à court terme ait été atteint en 1967 avec une survie de un an après l'opération. Malgré le développement important des techniques opératoires, la transplantation hépatique est restée au stade expérimental dans les années 1970, avec une survie des patients à un an avoisinant les 25%. L'introduction de la ciclosporine (développée par l'industrie bâloise) a nettement amélioré la survie des patients, si bien que les années 1980 ont vu la transplantation hépatique devenir le traitement de choix pour les adultes et les enfants atteints de maladies hépatiques chroniques ou fulminantes. Cette intervention est actuellement effectuée dans la plupart des grands centres universitaires d'Europe. A une année, la survie des patients est de 85 à 90%, et les résultats continuent de s'améliorer, même si la transplantation hépatique reste une procédure lourde, avec un certain risque de complications. Malheureusement, la disponibilité des organes susceptibles d'être greffés est de loin inférieure au nombre de bénéficiaires potentiels, une réalité qui a stimulé le développement de la transplantation hépatique «donneur vivant».
La transplantation hépatique est potentiellement applicable à toute situation aiguë ou chronique entraînant un dysfonctionnement hépatique irréversible, à condition que le bénéficiaire ne présente pas d'autres problèmes de santé qui s'opposeraient à une transplantation réussie. Le cancer du foie disséminé (métastatique), l'abus d'alcool actif, la présence d'infections opportunistes actives sont des contre-indications absolues. De nos jours, l'infection par le VIH n'est plus considérée comme une contre-indication absolue. L'âge avancé, ainsi que les maladies cardiaques ou pulmonaires graves, sont des contre-indications relatives à la transplantation. Les maladies chroniques du foie, induisant une cicatrisation excessive et irréversible du foie (cirrhose), sont la principale indication de la plupart des transplantations hépatiques. En cas de tumeur du foie non métastatique, les critères de Milan sont utilisés pour savoir quels patients qui pourront bénéficier d'une greffe de foie. En cas d'insuffisance hépatique majeure, il n'existe actuellement pas d'alternative à la transplantation. Néanmoins, des thérapies de soutien à la fonction hépatique peuvent éventuellement être entreprises (en attendant qu'un organe soit disponible), cependant ces supports externes au métabolisme du foie (dialyse par un foie bioartificiel) sont encore en cours d'évaluation préclinique et clinique.
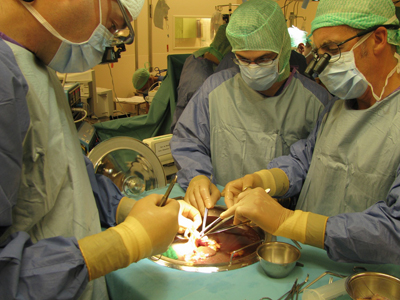 En général, la transplantation hépatique est effectuée de façon orthotopique. En d'autres termes, le foie malade est alors retiré et le foie du donneur (nouveau foie) est placé dans le même site anatomique.
En général, la transplantation hépatique est effectuée de façon orthotopique. En d'autres termes, le foie malade est alors retiré et le foie du donneur (nouveau foie) est placé dans le même site anatomique.
La transplantation est composées de quatre étapes : l'hépatectomie (ablation du foie malade), la phase anhépatique (sans foie), la phase d'implantation (mise en place du nouveau foie) et la phase post-implantation.
L'opération se fait par une grande incision au niveau de l'abdomen supérieur, sous les côtes et s'étendant principalement du côté droit). L'hépatectomie implique la dissection de toutes les attaches ligamentaires du foie, ainsi que de la voie biliaire principale, l'artère hépatique, les veines sus-hépatiques et la veine porte. Habituellement, la partie rétrohepatique de la veine cave inférieure est retirée avec le foie, bien qu'une autre technique puisse la préserver (technique dite "piggyback").
Le sang du donneur présent dans le foie sera vidé et remplacé par une solution de stockage réfrigérée spécialement conçue pour la préservation d'organes. L'implantation de ce nouveau foie implique des anastomoses (connexions) de la veine cave inférieure, la veine porte et l'artère hépatique. Une fois que le flux sanguin est rétabli dans le nouveau foie, les voies biliaires (canal cholédoque) sont anastomosées (connectées) à l'intestin grêle. L'intervention dure habituellement entre cinq et six heures, mais peut être plus ou moins longue en raison de la difficulté de l'opération et l'expérience du chirurgien.
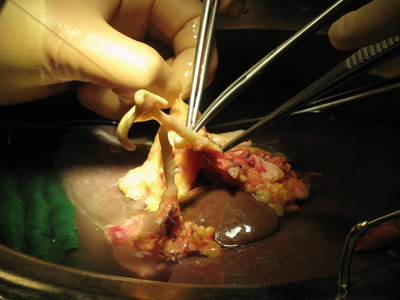
La grande majorité des greffes de foie utilisent le foie entier d'un donneur non-vivant, en particulier pour les receveurs adultes. Une avancée majeure en transplantation hépatique pédiatrique a été le développement d'une technique permettant de réduire la taille du greffon, dans laquelle seule une partie du foie d'un adulte est utilisé pour un bébé ou un petit enfant. On utilise donc la technique dite du «split», où le foie est séparé en deux, la partie gauche (plus petite) permettant de greffer un enfant, et la partie gauche (plus volumineuse) permettant de greffer un adulte. La transplantation hépatique peut également être réalisée à partir d'un donneur vivant. Une partie du foie d'une personne en bonne santé est ainsi retiré et utilisé comme greffe pour un enfant (en générale un lien familial lie le donneur adulte au receveur pédiatrique. On procède à l'ablation d'environ 20% du foie du donneur adulte (partie gauche). Cette partie régénère dans les quelques semaines qui suivent.
Comme la plupart des allogreffes d'autres organes, une greffe du foie sera rejetée par le bénéficiaire à moins que des médicaments immunosuppresseurs soient utilisés. Les traitements immunosuppresseurs pour les différentes transplantations d'organes sont relativement similaires, plusieurs médicaments anti-rejets sont maintenant disponibles. La plupart des greffés du foie reçoivent des «corticostéroïdes» (cortisone) associé à un «inhibiteur de la calcineurine» tels que la ciclosporine ou le tacrolimus, avec en plus un «antimétabolite» comme le mycophénolate mofétil.
La transplantation hépatique est unique en ce qui concerne le risque de rejet, car celui-ci diminue au fil du temps, cependant les bénéficiaires ont besoin de prendre des médicaments immunosuppresseurs pour le reste de leur vie. Le foie est actuellement étudié pour son rôle dans la maturation de certaines cellules se rapportant au système immunitaire, ce qui pourrait expliquer sont statut privilégié face au rejet.
Après une greffe du foie, trois types de rejet peuvent se produire: le rejet hyperaigu, le rejet aigu et le rejet chronique. Le rejet hyperaigu est causé par des anticorps anti-donneurs préformés, c'est-à-dire que le receveur a été exposé au préalable à des antigènes (protéines) similaires à celles du donneur. Le rejet hyperaigu se passe dans les minutes ou heures après la procédure de transplantation. Il est actuellement rarissime en raison des tests effectués avant la greffe (crossmatch). Le rejet aigu est la plus fréquente et la principale cible des agents immunosuppresseurs. Le rejet aigu est généralement observé dans les jours ou semaines qui suivent la transplantation. Le rejet chronique est la présence de tout signe et symptôme de rejet, un an après la transplantation. La cause du rejet chronique est encore inconnue, cependant un rejet aigu augmente le risque de survenue d'un rejet chronique. Le rejet du foie peut survenir à tout moment après la greffe, c'est pourquoi les valeurs des enzymes hépatiques doivent être contrôlées régulièrement. Les signes du rejet comprennent également, l'encéphalopathie, une jaunisse, des ecchymoses et une tendance aux saignements. Il existe également des présentations non spécifiques comme des malaises, une anorexie, des douleurs musculaires, une fièvre et une légère augmentation du nombre de globules blancs.
 Le pronostic est assez bon. Toutefois, il dépend du type de maladie qui a conduit à la transplantation. Il n'existe pas de modèle exact pour prédire les taux de survie, ceux qui bénéficient d'une greffe ont une chance de survie de 58% à 15 ans. Une défaillance du nouveau foie survient chez 10% à 15% des patients. L'échec de la greffe est parfois dû à une maladie préexistante dans l'organe donné (par exemple en cas d'hépatite C). D'autres problèmes sont les complications survenant pendant l'opération (problème dans la connexion des différents vaisseaux), elles peuvent conduire à une greffe non fonctionnelle.
Le pronostic est assez bon. Toutefois, il dépend du type de maladie qui a conduit à la transplantation. Il n'existe pas de modèle exact pour prédire les taux de survie, ceux qui bénéficient d'une greffe ont une chance de survie de 58% à 15 ans. Une défaillance du nouveau foie survient chez 10% à 15% des patients. L'échec de la greffe est parfois dû à une maladie préexistante dans l'organe donné (par exemple en cas d'hépatite C). D'autres problèmes sont les complications survenant pendant l'opération (problème dans la connexion des différents vaisseaux), elles peuvent conduire à une greffe non fonctionnelle.
La transplantation hépatique dite « donneur vivant » a émergé dans les dernières décennies comme une option thérapeutique alternative pour les patients présentant une maladie hépatique au stade terminal. Les principales indications à un tel geste sont la cirrhose ou le carcinome hépatocellulaire (cancer du foie), ces derniers sont souvent imputables à un ou plusieurs des éléments suivants: l'abus d'alcool au long cours, ainsi que l'hépatite C et l'hépatite B non traitées et ceci après plusieurs décennies d'évolution. Le concept de la transplantation hépatique « donneur vivant » a émergé en réponse à la pénurie généralisée de foies de donneurs décédés, et s'est révélée possible grâce à la remarquable capacité de régénération que possède le foie humain. Durant cette opération, un morceau de foie sain est prélevé sur une personne vivante et transplanté au receveur après que le foie malade ait été enlevé.
Historiquement, la transplantation hépatique « donneur vivant » fut en premier lieu l'alternative pour les d'enfants atteints d'une maladie hépatique grave. Elle permit à l'un des deux parents d'offrir une partie de son foie à son enfant, permettant ainsi d'éviter les complications dramatiques survenant durant l'attente d'un organe disponible.
La première transplantation hépatique « donneur vivant » a été réalisée avec succès par le Dr Christoph Broelsch, au Centre Universitaire de Chicago en novembre 1989, lorsqu'une fillette de 2 ans, Alyssa Smith, a reçu une partie du foie de sa mère. Plus tard, la transplantation hépatique « donneur vivant » s'est révélée possible également d'adultes à adultes, et est maintenant pratiquée dans quelques grands centres universitaires. Elle est considéré comme techniquement plus exigeante que la transplantation d'un foie de donneur décédé et pose également des problèmes éthiques inhérents à la réalisation d'une opération chirurgicale majeure (hépatectomie) sur un être humain en bonne santé.
Dans une étude récente, le risque de complications chez le donneur vivant est d'environ 10%, cependant, une seconde opération n'est qu'exceptionnellement nécessaire. Les complications courantes sont les fistules biliaires, la stase gastrique et les infections postopératoires. Elles sont plus fréquentes si l'on prélève le lobe droit du foie. Le décès après la transplantation hépatique « donneur vivant » est actuellement de moins de 1% (0% au Japon et 0,3% aux USA).
Habituellement, il est possible de prélever 55 à 70% du foie (le lobe droit) d'une personne en bonne santé sans risquer de complications majeures. Après l'intervention, le foie du donneur se régénère rapidement, si bien que sa fonction redevient normale dans les semaines qui suivent. Le foie retrouve sa taille initiale en quelques mois. Le retour à une taille et fonction normale mettra plus de temps chez le receveur.
Les donneurs vivants sont exposés à des risques et complications éventuelles après l'opération. Par exemple, des caillots de sang peuvent se former dans les voies biliaires et provoquer un ictère (jaunisse). Cependant, ces complications sont traitables sans nécessiter une ré-intervention. Bien qu'il existe un risque de mortalité pour le donneur, celui-ci reste très faible, voire inexistant dans certains centres.
Tout membre de la famille, parent, frère ou sœur, enfant, ou conjoint peut faire don de son foie. Les critères d'un don du foie comprennent:
Avant de devenir donneur, toute une série de test est effectuée. Un scanner ou une IRM permettent d'obtenir une image précise du foie du receveur. Dans la plupart des cas, ces examens prennent entre deux et trois semaines. Les frais des examens pré- et post-opératoires ainsi que l'opération elle-même sont intégralement pris en charge par l'assurance maladie du receveur.
Très peu de personnes nécessitent une transfusion sanguine pendant ou après la chirurgie. Même si cette intervention est très sûre, tous les donneurs potentiels devraient connaître le risque de décès qui est de 0 à 0.5%. Les autres risques de don du foie, sont notamment les saignements, les infections, une incision douloureuse, la possibilité de formation de thrombose dans les vaisseaux anastomosés et une longue convalescence. La grande majorité des donneurs récupèrent complètement et durablement de l'opération dans les deux à trois mois.
Les avantages de la transplantation hépatique « donneur vivant » sur la transplantation avec « donneur décédé » sont:
La greffe peut être faite de manière élective
Il y a un moins de complications et de décès (car on évite ceux qui surviennent pendant l'attente d'un organe de donneur décédé)
La qualité de préservation de l'organe est optimale (le temps de transport du donneur au receveur est très court)
La réaction de rejet peut être diminuée (en cas de parenté directe)
Sélection des donneurs
La majorité des centres de transplantation hépatique affiche d'excellents résultats sur la survie des patients à long terme. Le don vivant d'un organe est une approche multidisciplinaire. Tous les donneurs de foie doivent subir une évaluation médicale complète. Dans le Service de Chirurgie Viscérale et Transplantation des Hôpitaux Universitaires de Genève, il existe une équipe médico-soignante spécialisée en transplantation qui est à même de donner des informations spécifiques sur l'intervention et de répondre aux questions que les familles peuvent avoir. Le processus d'évaluation du donneur est strictement confidentiel, même vis-à-vis du receveur. Tous les efforts sont faits pour s'assurer que le don d'organes ne se fait pas par la contrainte d'autres membres de la famille. L'équipe de transplantation fournit à la fois au donneur et au receveur, ainsi qu'aux membres leur famille, les conseils approfondi et le soutien nécessaire tout au long du processus de guérison.
Pour en savoir plus sur la transplantation hépatique aux HUG, vous pouvez consulter :